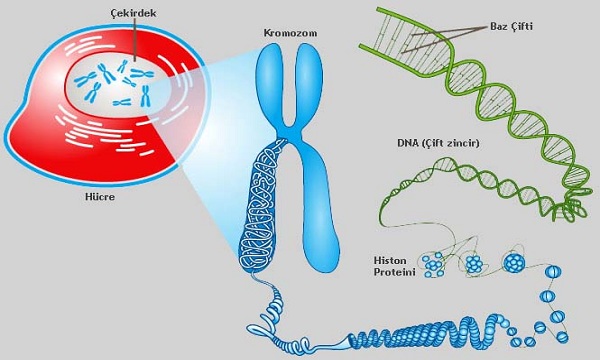
Histonlar, DNA’yı düzgün bir şekilde kromozomlara yoğunlaştıran ve paketleyen proteinlerdir. Bu proteinlerdeki değişiklikler, transkripsiyonun aktivasyonu / inaktivasyonu, kromozom ambalajlaması, DNA hasarı ve DNA onarımı gibi hücre içindeki farklı süreçleri etkiler. Histonların modifikasyonu, gen ifadesinde önemli bir rol oynayan önemli bir çeviri sonrası süreçtir. Modifikasyonlar, bu gen ekspresyonunu kromatin yapısını değiştirerek veya histon değiştiricilerin işe alımını etkileyerek etkiler.
Histonlar, DNA molekülünü çekirdeğe sığdırmak için DNA’yı nükleozom olarak adlandırılan yapılara paketler. Bu nükleozomların her biri, her biri H2A, H2B, H3 ve H4 histonik histonlarını ve stabilizör olarak etkiyen H1 olarak adlandırılan bir bağlayıcı histonu içeren iki alt birime sahiptir. Aşağıdaki bölümlerde, üç önemli histon modifikasyonu kısaca tartışılmaktadır.
Histon Asetilasyonu
Histon asetilasyonu, gen ekspresyonunu arttıran transkripsiyon faktörlerine açık ve bu nedenle erişilebilir bir kromatin yapısı ile büyük ölçüde ilişkilidir. Büyük ölçüde destekleyici bölgelere hedeflenmektedir. Örneğin, genellikle H3 üzerinde asetilasyon, aktif gen geliştiriciler ve promoterler ile ilişkilidir.
Histon kuyruklarının asetilasyonunu düzenlemekten sorumlu enzimler, histon asetiltransferazlar (HATs) ve histon deasetilazlardır (HDAC’ler). HAT’lar için tercih edilen hedefler histon H3 ve H4’ün kuyruklarındaki lisin kalıntılarıdır. Histon asetilasyonu tersine çevrilebilir bir reaksiyondur. HDAC’ler, asetil gruplarının histon lizin kalıntılarından çıkarılmasını sağlar.
Histon asetilasyonundaki bir dengesizlik, tümör oluşumu ve kanser progresyonuna bağlanmıştır. H3’ün lisin kalıntısında asetile edilip edilmediğini belirleyebilmek, asetilasyon paternlerini karakterize etmek ve araştırmacıların gen ekspresyonunun epigenetik tarafından nasıl düzenlendiğini ve ayrıca HAT-hedefli ilaçların gelişimine nasıl yardımcı olduğunu anlamalarına yardımcı olabilir.
Histon Metilasyonu
Histon metilasyonu, bir ila üç metil grubu olan S-adenosil-L-metiyoninin, histon proteinlerinin lisin veya arginin kalıntılarına aktarılmasıdır. Aktarım, histon metil transferazlar (HMT’ler) ile katalize edilir. Metilasyon bölgesine bağlı olarak, H3 ve H4’teki lizinin metilasyonu, hem transkripsiyonun aktivasyonunda hem de baskılanmasında rol oynar, ancak arginin metilasyonu sadece transkripsiyonun aktivasyonunda rol oynar. Kalıntılar, lisin metiltransferazlar adı verilen enzimlerin yardımıyla metillenir. Tek tek metilasyon bölgelerine fonksiyonel çeşitlilik, lisinin mono-, di- veya trimetillenmesiyle sağlanır.
Örneğin, K4’ün histon H3 üzerinde hem mono- hem de tri-metilasyonu transkripsiyonel aktivasyona neden olmakta, fakat ilk önce transkripsiyon arttırıcılarda ortaya çıkmakta ve ikincisi gen promoterlerinde gerçekleşmektedir. K9 ve K27’nin histon H3 üzerindeki tri-metilasyonu, transkripsiyonun baskılanması için bir işarettir. K27’nin trimetilasyonu esas olarak gen bakımından zengin kromozomal bölgelerdeki promotörlerde ortaya çıkar ve embriyoların kök hücrelerinde gelişim düzenleyicilerini kontrol ederken, K9’un trimetilasyonu genellikle telomerler veya uydu tekrarları gibi gen zayıf bölgelerinde görülür.
Histon Fosforilasyonu
Hücre bölünmesi, DNA onarımı ve transkripsiyonel düzenleme gerçekleşirken, çekirdek histonların fosforilasyonu kromozom yoğunlaşması için çok önemlidir. Histon kinazları, ATP’den bir hedef amino asit yan zincirinin hidroksil grubuna alınan bir fosfat grubunu ekler. Histon fosforilasyonu diğer histon modifikasyonları arasındaki etkileşimleri arttırır ve efektör proteinleri için bir platform sağlar.
Kromatinin sıkıştırılması ve yapısının düzenlenmesi ve mitoz sırasında işlev görmesi için H2O’da T120’de H2O ve S10’da H3’teki histon fosforilasyonu gereklidir.






 Alıntı ile Cevapla
Alıntı ile Cevapla